採血管は「DNAか細胞か」で選ぶ|使い分けの基本
採血管は、調べたい対象が「DNAか細胞か」で選びます。
- PCR・DNA検査 → EDTA
- 細胞機能・フロー → ヘパリン
- 採血順序を守らない → 結果は壊れる
この3つを押さえるだけで、現場でのミスの大半は防げます。
採血管は色で覚えるより、目的で選ぶのが基本です。
採血管は“検査の前処理”であり、ここでミスると後工程はすべて崩れます。
採血管の選択ミスで起こるトラブル
採血管のトラブルの多くは、
- PCRがうまくいかない
- 細胞が反応しない
- 検査値がおかしい
といった「原因が見えにくい問題」です。
そしてその原因はシンプルで、採血管の選択ミスです。
採血管の基本ロジック(まず全体像)
EDTA管(紫)
- Caをキレート → 凝固を止める
- DNAを安定に保つ
- PCRを邪魔しない
DNA検査・PCR向き
ヘパリン管(緑)
- 抗凝固作用あり
- 細胞の機能を保ちやすい
- ただしPCRを阻害する
生細胞を使う検査向き(刺激試験・フローなど)
よくある失敗7選
① ヘパリン血でPCRしてしまう
→ PCRはEDTAが基本
ヘパリンはDNAポリメラーゼの働きを阻害するため、PCRがうまく増幅されないことがあります。その結果、増幅効率の低下や偽陰性の原因になります。
DNA検査やPCRにはEDTA管を使用するのが基本です。
※ヘパリンは陰性電荷を持ち、酵素反応を妨げる
② 刺激試験でEDTA血を使う
→ 細胞機能検査はヘパリンが基本
EDTAはカルシウムをキレートするため、細胞のシグナル伝達が阻害されます。
その結果、刺激を与えても細胞が反応しないことがあります。
細胞機能を評価する検査では、ヘパリン血を使用します。
※カルシウムは細胞内シグナルに必須
③ 採血順序を守らない
→ 採血の順番を守る=汚染防止
採血順序を守らないと、他の採血管の抗凝固剤が混入し、検査値に影響を与えます。
特にEDTAは影響が強く、少量でも結果を大きく変えてしまいます。
採血は決められた順序で行い、試薬の持ち込み汚染を防ぐことが重要です。
※EDTA混入はCa低値などの原因になる
④ 転倒混和ミス
→ 採血管ごとに決められた回数でやさしく転倒混和
転倒混和は、採血管ごとに決められた回数でやさしく行います。
混和不足は凝固、混ぜすぎは溶血の原因になります。
例)
・EDTA/ヘパリン:8〜10回
・クエン酸:3〜4回
・血清:5回程度
※転倒混和は「振る」のではなく、ゆっくり上下反転させる操作です
⑤ 採血量不足
→ 規定量を守る
採血量が不足すると、抗凝固剤との比率が崩れ、正しい検査結果が得られなくなります。
クエン酸管は採血量のズレがそのまま測定誤差になるため注意が必要です。
採血は規定量を守ることが重要です。
※クエン酸管は血液:抗凝固剤=9:1が前提
⑥ EDTAの種類を意識しない
→ 基本は施設ルールに従う
EDTAにはNa、K2、K3などの種類があり、使用する塩によって検査値に影響が出る場合があります。
特にK塩はカリウム測定に影響する可能性があります。
採血管の種類は施設ルールに従って使用します。
※検査項目によって指定されることがある
⑦ 検体放置
→ 速やかに処理する
採血後に検体を放置すると、細胞の状態が変化し、正しい結果が得られなくなります。
時間の経過とともに細胞死や機能低下が進みます。
検体は速やかに処理することが重要です。
※細胞機能検査では特に影響が大きい
⑧ 温度管理ミス
→ 冷やせばいいわけではない
血液は検査によって適切な保存温度が異なります。
特に細胞系検査では冷蔵により機能が低下するため注意が必要です。
※当日できない場合は冷蔵されることが多いが、保存時間は検査ごとに異なる
現場で迷う例外パターン
フローサイトメトリーはどっちでもいい?
→ 目的によって使い分ける
フローサイトメトリーは一律に「どちらでも良い」わけではなく、
何を評価するかで採血管が決まります。
表面マーカー(CD抗原など)を解析する場合は、EDTA血でも問題なく実施可能です。
一方で、細胞の機能(刺激試験やシグナル解析)を評価する場合は、
EDTAによってカルシウムがキレートされ、細胞が反応しなくなるため、
ヘパリン血が推奨されます。
例)
・表面マーカー解析 → EDTAでも可
・細胞機能評価 → ヘパリン
DNA抽出だけならヘパリンでもいい?
→ 抽出は可、PCRはNGの可能性あり
DNA抽出自体はヘパリン血でも可能です。
ただし、ヘパリンはDNAポリメラーゼの働きを阻害するため、PCRでは増幅できないことがあります。
また、採血量が不足するとヘパリンの影響が相対的に強くなり、さらにPCRがうまくいかなくなることがあります。
PCRと細胞検査が両方あるときの判断
PCRと細胞検査が同時に必要な場合は、
「どちらが失敗すると取り返しがつかないか」で判断します。
例えば、
- PCRはヘパリン血ではうまくいかない
- 一方、表面マーカーのフローはEDTAでも実施できる
この場合はPCRを優先し、EDTAを選びます。
一方で、
- PCRもEDTAが必要
- 細胞機能検査もヘパリンが必要
というように、どちらも代替できない場合は、
再採血が可能かどうかを最優先で判断します。
採血順序はなぜ重要か
採血順序の本質は試薬の持ち込み汚染を防ぐためのルールです。
採血管は「他の検査に影響を与えやすいものを後ろに回す」順番で採取します。
一般的な採血順序
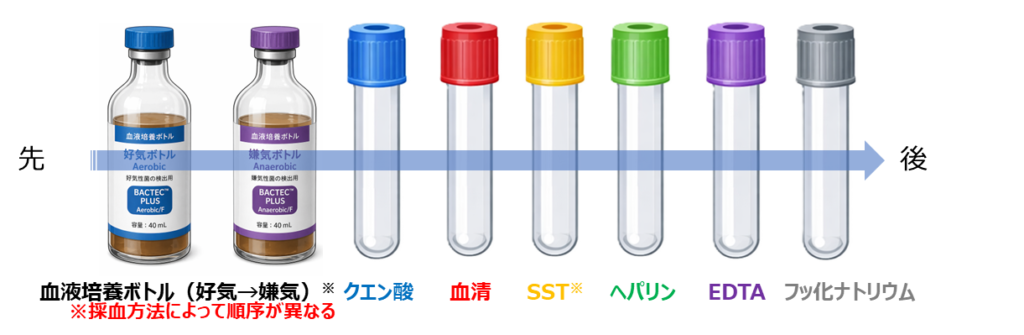
※施設によって異なる場合があります。
血液培養だけは別物
血液培養は専用ボトルを使用し、細菌の有無を調べます。
そのため、他の採血管とは目的が異なり最優先で採取されます。
血液培養ボトルの採血順序
→ 採血方法で順序が変わることに注意が必要です。
血液培養は、好気ボトルと嫌気ボトルの2本を使用するのが基本です。
これは、空気を好む菌(好気性菌)と、空気を嫌う菌(嫌気性菌)の両方を検出するためです。
血液培養ボトルは、採血方法によって順序が異なります。
・シリンジ採血:嫌気 → 好気
・直接採血(翼状針など):好気 → 嫌気
一般的な臨床現場では直接採血が多いため、
好気ボトルを先に採取するケースが多くなります。
血液培養は通常の採血管とは異なり、専用ボトルで細菌の有無を調べる検査です。
※十分な血液量をそれぞれのボトルに分けて入れることが重要です。
なぜこの順番?
EDTAが最後の理由
→ Caを強力にキレートし、他検査に大きく影響するため
クエン酸が前の理由
→ 凝固検査は微量の混入でも結果が変わるため
ヘパリンが中間の理由
→ 影響はあるがEDTAほど強くないため
フッ化ナトリウムが最後の理由
→ 酵素反応を止めるため、他検査に影響するため
採血管は“後ろに行くほど他検査への影響が大きい”と考えると理解しやすい
よくあるミス
- EDTAを先に取る → Ca低値
- クエン酸後回し → 凝固検査ズレ
- 順番無視 → 原因不明の異常
まとめ
採血管は丸暗記ではなく、
- PCRをするのか
- 細胞を使うのか
で判断します。
さらに、
- 採血順序
- 検体の取り扱い(時間・量)
まで含めて考えることで、現場でのミスは大きく減らせます。
今日のおさらい
~ちょっと考えてみよう~
Q1:PCRに向く採血管はどれ?
Q2:ヘパリンがPCRに向かない理由は?
Q3:採血順序を守らないと何が起きる?
答え
A1:EDTA
A2:DNAポリメラーゼの働きを阻害するから
A3:検査結果が正しく出ない

