前回は「血液を固めて得られる血清」について解説しました。
では逆に、血液を固めずに遠心した場合、上澄みはどうなるのでしょうか?
それが「血漿(plasma)」です。
ここで多くの人が疑問に思います。
「同じ血漿なのに、なぜ採血管を使い分けるのか?」
この記事では、この疑問を軸に血漿の正体と、抗凝固剤による違いを整理します。
血漿とは何か?
血漿(plasma)とは、
抗凝固剤入りの採血管で採取した血液を遠心分離して得られる液体成分です。
血液を固めずに遠心すると、血液は大きく3つの層に分かれます。
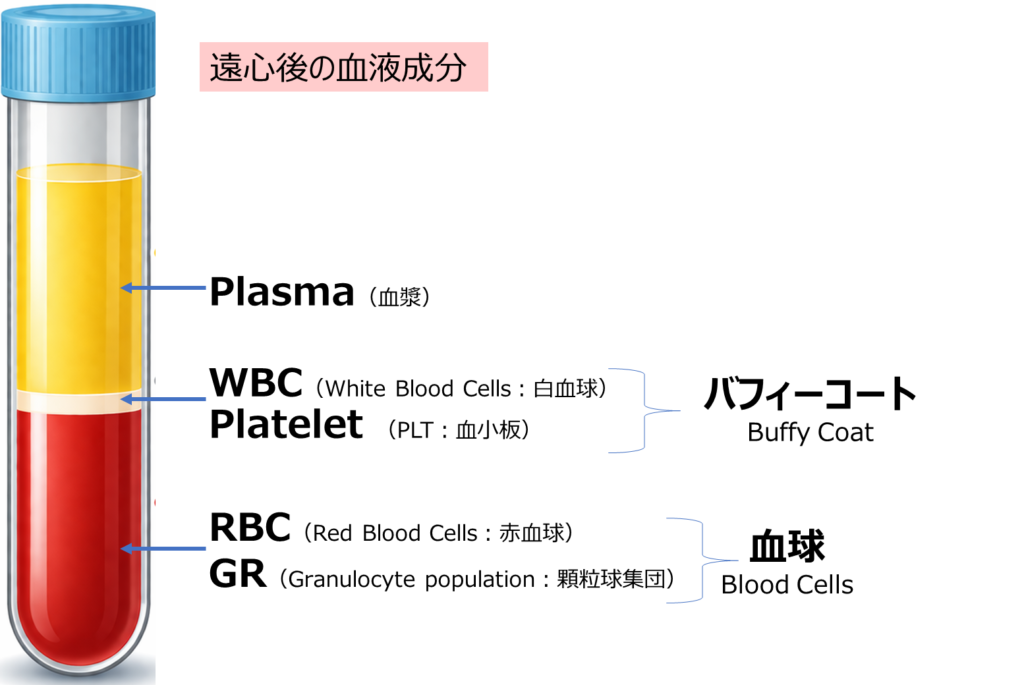
血液が固まらないのは、採血管の中に
**抗凝固剤(anticoagulant)**が入っているためです。
抗凝固剤は、血液の「固まる仕組み(凝固反応)」を止めることで、
血液を液体のまま保ちます。
👉止血の仕組みについての詳細はコチラ
血液はなぜ固まるのか?|出血を止める仕組みをやさしく解説
血清との違い
血漿と血清の最も大きな違いは、
凝固因子(フィブリノーゲン)を含むかどうかです。
- 血漿:凝固因子を含む
- 血清:凝固因子を含まない
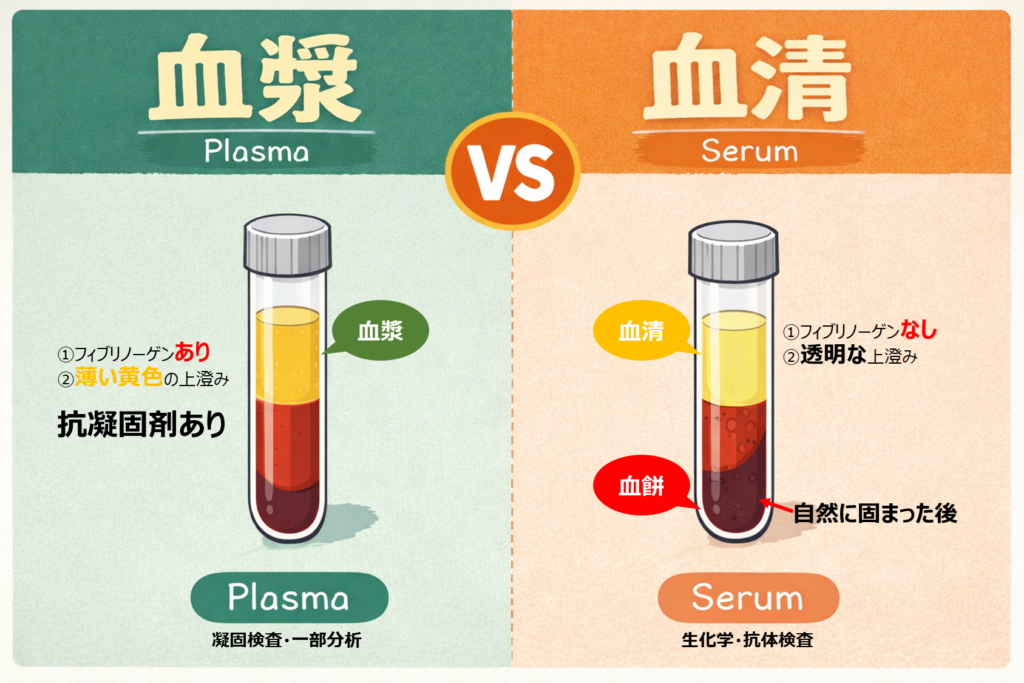
血液を固めると、フィブリノーゲンはフィブリンとして消費され、
上清(血清)には残りません。
一方、血液を固めずに遠心すると、凝固因子はそのまま残ります。
見た目は似ていても、中身はまったく異なります。
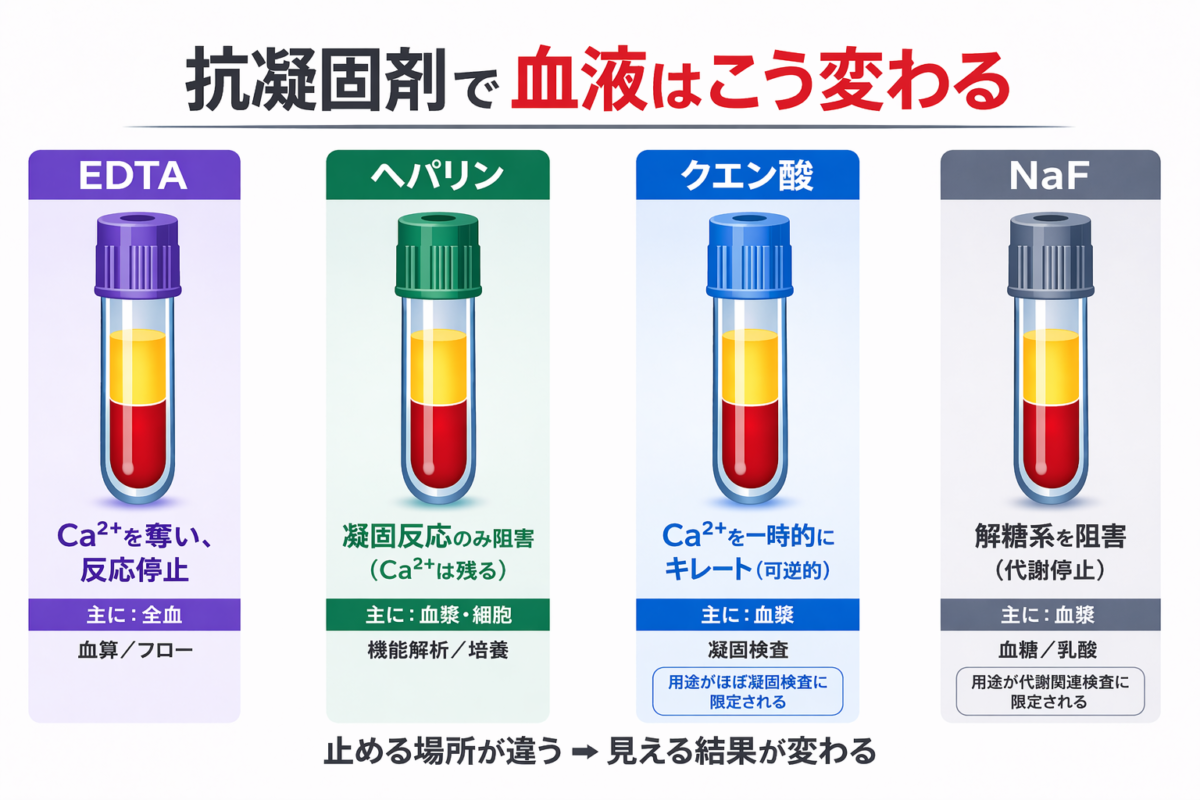
抗凝固剤で何が変わるのか?
血液凝固は、カルシウム(Ca²⁺)と凝固反応の連鎖によって起こります。
抗凝固剤は、この仕組みのどこかを止めることで血液の凝固を防いでいます。
そのため、どの反応を止めるかによって血漿の性質が変わるのがポイントです。
代表的な採血管用添加剤4種類
EDTA:カルシウムを強くキレート
ヘパリン:アンチトロンビンの作用を高め、トロンビンやXa因子などを抑制
クエン酸:カルシウムを一時的にキレート(可逆的)
NaF:解糖系を阻害(代謝抑制目的)
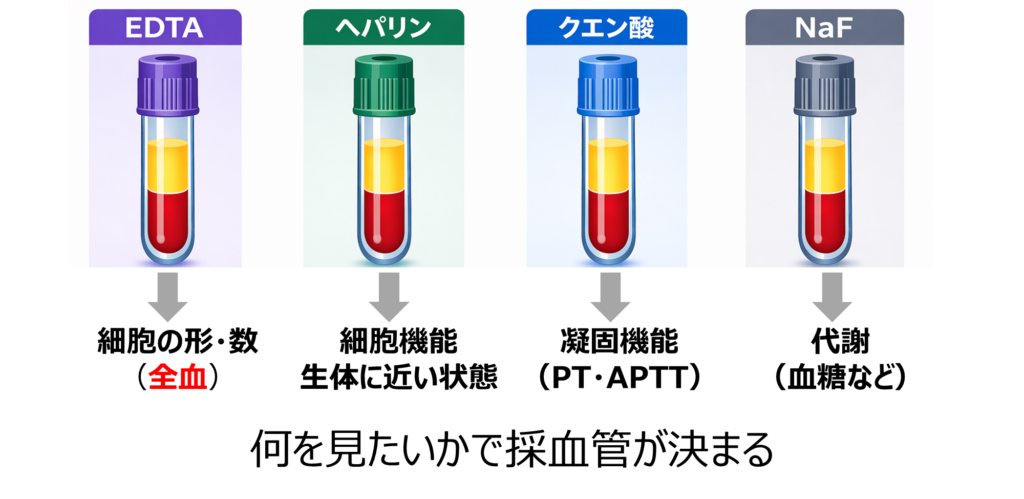
なぜ使い分けるのか?
血液中の何を調べたいかで採血管を使い分けます。
EDTAとヘパリン(現場でよく使う2つ)
実際の検査現場では、特にこの2つがよく使われます。
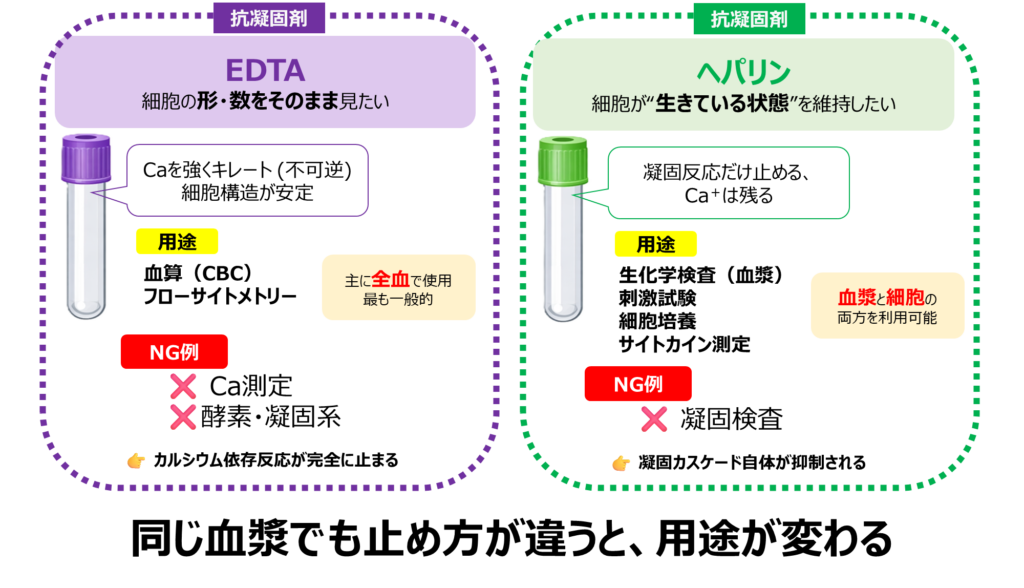
細胞の形・数を見たい → EDTA
- 血算(CBC)
- フローサイトメトリー
EDTAはカルシウムを強くキレートし、
反応を停止させることで細胞の状態を安定に保ちます。
主に全血で使用されるのが基本です。
一方で、Ca依存反応が止まるため、酵素反応や細胞機能の評価には一般的に向きません。
細胞機能・状態を保ちたい → ヘパリン
- 生化学検査(血漿)
- 細胞培養
- サイトカイン測定
ヘパリンは凝固反応のみを抑え、カルシウムは残ります。
そのため、血漿と細胞の両方を利用できるのが特徴です。
多くの生化学検査で使用されることがあり、
生体に近い状態を反映しやすいとされることがあります。
※ただし、測定項目によってはヘパリンが影響する場合もあります。
EDTA vs ヘパリンの本質的な違い

クエン酸・NaF(用途が限定される採血管)
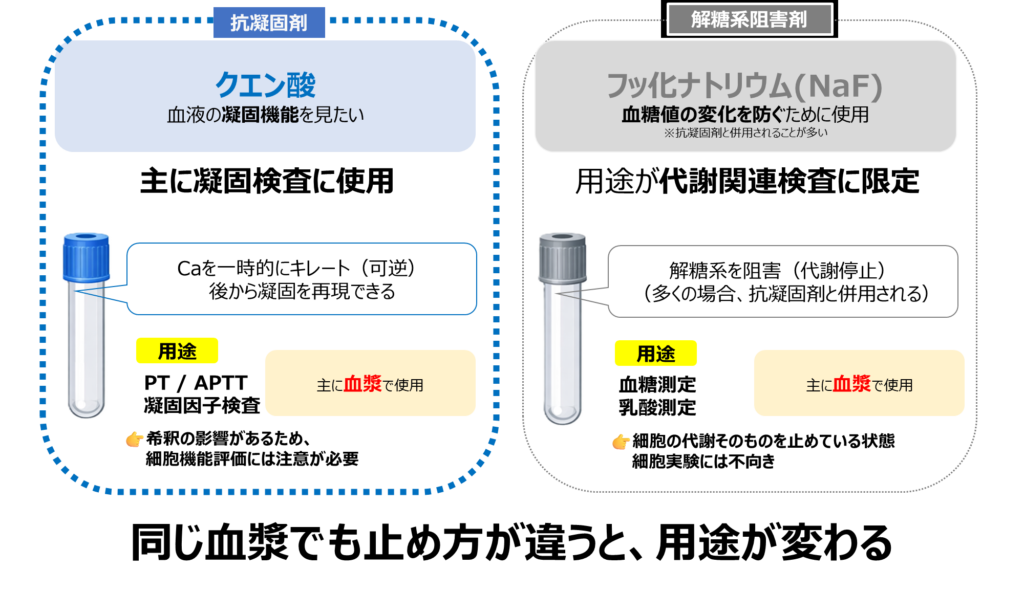
凝固機能を見たい → クエン酸
- PT / APTT
クエン酸はカルシウムを一時的にキレートし、
後から再び凝固を起こせる(可逆的)ことが特徴です。
用途はほぼ凝固検査に限定されます。
また、液体試薬が入っているため血液が希釈される点にも注意が必要です。
血糖代謝を見たい → NaF
- 血糖測定
- 乳酸測定
NaF(フッ化ナトリウム)は、解糖系を阻害して血糖の変化を防ぐために使用されます。
解糖とは、細胞が糖(グルコース)を消費する反応のことです。
血液中の細胞は採血後も糖を消費するため、この変化を抑える目的で用いられます。
NaFは抗凝固剤ではなく、代謝を止める試薬です。
多くの場合、EDTAやシュウ酸などの抗凝固剤と併用されます。
用途は代謝関連検査にほぼ限定されます。
※HbA1cは血液中の糖ではなく、赤血球内のヘモグロビンに結合した糖を測定するため、
血糖の変化を防ぐNaFは通常使用されません。
※細胞の代謝を停止させるため、細胞機能評価や分離には一般的に不向きです。
補足:免疫系検査での違い
サイトカイン(IL-6、TNF-αなど)は、血清と血漿で値が異なることがあります。
これは、凝固過程で血小板や白血球が活性化し、サイトカインが放出されるためです。
一般的には、血漿(特にヘパリン)がより生体に近い状態を反映しやすいとされることがあります。
PBMC分離と採血管の使い分け
PBMC分離自体は、EDTAでもヘパリンでも可能です。
ただし、細胞機能評価を行う場合はヘパリンが選ばれることが多いという違いがあります。
またフローサイトメトリーについても、
- 表面マーカー解析 → EDTAでも可
- 機能解析・培養前提 → ヘパリンが有利
といった使い分けが行われます。
👉PBMC分離についてはコチラの記事で詳しく解説しています。
リンフォプレップ(Lymphoprep)とは?PBMC分離の原理・使い方・よくある失敗まで解説
現場での実際の運用
検査は1つの検体に複数の目的が含まれることがあります。
例えば:
- フローサイトメトリー
- 細胞培養
が同時に依頼された場合、ヘパリン管を優先し、血漿回収後にPBMC分離を行う、
といった運用がされます。
一方で、現場ではEDTA管が最も多く使われます。
理由は、血算(CBC)がルーチン検査の中心のため、
採血時に標準的に使用されるからです。
そのためEDTAは「全血でそのまま使う」採血管です。
イメージ(例え)
血液を「具(細胞)だくさんのスープ(血漿)」に例えると:
- EDTA:スープごと“動きを止める”
- ヘパリン:スープと具を分けて、それぞれ使える
- クエン酸:スープの“固まりやすさ”を調べる
- NaF:スープの“成分変化(糖など)”を止める
同じ血液でも、止め方によって使い道が変わります。
まとめ
- 血漿は「血液を固めずに得られる上清」
- 凝固因子(フィブリノーゲン)を含む
- 抗凝固剤によって性質が変わる
採血管は「何を見たいか」で決まります。
- 細胞の形・数 → EDTA
- 細胞機能 → ヘパリン
- 凝固機能 → クエン酸
- 代謝(血糖など) → NaF(※補足的)
同じ血漿でも、前処理が違えば別物になります。
今日のおさらい
~ちょっと考えてみよう~
Q. フローサイトメトリーにはどの採血管が向いている?
→ EDTA(※表面マーカー解析の場合)
Q. 細胞培養を行う場合は?
→ ヘパリン
Q. 凝固検査に使うのは?
→ クエン酸
最後に
※本記事の内容は一般的な臨床検査・研究現場での傾向に基づいています。
検査内容や施設によって、使用する採血管は異なる場合があります。