フローサイトメトリーを行う際には、
「どれくらいの細胞が手元にあって、そのうちどれだけを実験に使うのか」
を計算する必要があります。
しかし、この計算は初学者にとって大きな壁です。
私は初めてフローサイトメトリーを教わったとき、
先輩が顕微鏡をのぞきながら細胞を数え、さらっと暗算している姿を見て、
「何のために、何を計算しているのか?」
がまったく分かりませんでした。
カウントした数字が、どのように「必要な細胞数(例:2×10⁶個)」に変換されるのか、
頭の中でつながらなかったのです。
この記事では、
- 細胞カウントの基本(チュルク液・血球計算盤)
- カウント値から細胞濃度を求める方法
- 必要な細胞数(2×10⁶個)に合わせて分取・濃縮する考え方
について、実際につまずいた視点からやさしく解説します。
細胞数のカウントとは何か
まず前提として、フローサイトメトリーではPBMC層を取り出したあと、
すべての細胞をそのまま検査に使うわけではありません。
まず、その検体からどのくらいの細胞が得られたのか、
「1 mLあたり何個の細胞があるか(細胞濃度)」を確認し、
必要な細胞数(例:2×10⁶個)になるように調整(希釈・濃縮)する必要があります。
そこで最初に行うのが、細胞数のカウントです。
細胞はそのままでは数えにくいため、分取した細胞の一部を染色液で染色し、**血球計算盤(ヘモサイトメーター)**に入れて、顕微鏡で観察しながら細胞数を数えます。
細胞をカウントするときは、下図のように血球計算盤の赤い点線で囲った一区画(大区画)を使用します。
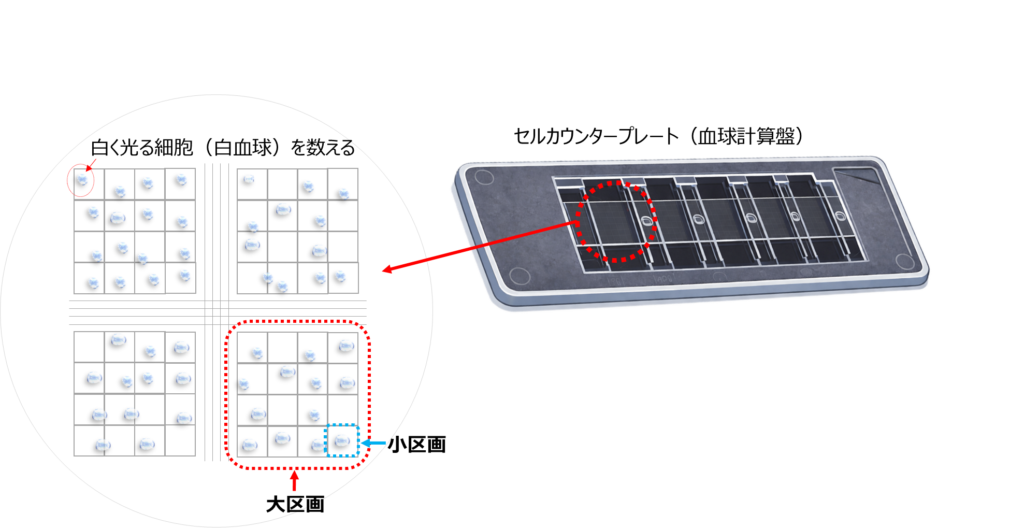
顕微鏡で観察すると、血球計算盤は
4つの大きな区画(大区画)と、それを構成する小さな区画(小区画)
に分かれていることが分かります。
細胞の具体的な数え方や使用する染色液については別の記事で詳しく解説しますが、
本記事では、「細胞がどのように見えているのか」をイメージしてもらうために、この図を掲載しています。
細胞の染色液とカウント方法は別の記事で詳しく解説します。
👉血球計算盤の数え方|境界ルールとカウントミスを防ぐコツ
血球計算盤と希釈の基本
ここで重要になるのが、希釈の考え方です。
細胞はそのままでは数えにくいため、染色液(例:チュルク液など)で希釈してからカウントします。
希釈倍率に厳密な決まりはありませんが、今回は例として
- 染色液:30 μL
- 細胞溶液:10 μL
とします。
この場合、全体は40 μLとなるため、細胞は4倍に希釈されているということになります。
この「4倍希釈」という情報は、後で細胞濃度を計算するときに必ず必要になります。
次のステップでは、実際に血球計算盤で数えた値(例:110個)から、
「1 mLあたりの細胞数(cells/mL)」を求めます。
血球計算盤1マスの体積
血球計算盤の1マスは、平面のマス目として見えますが、実際には深さを持った立体構造になっています。
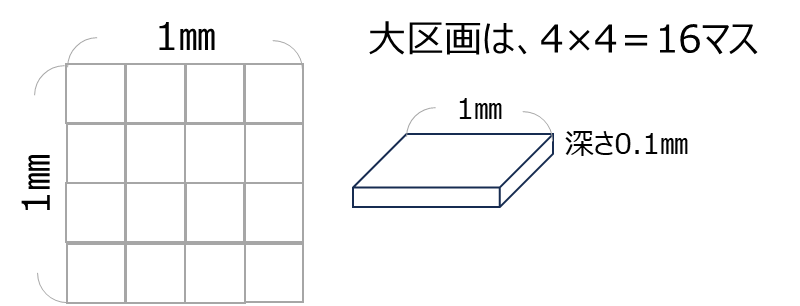
左の図は、顕微鏡で見えるマス目(上から見た図)です。
一方で右の図は、そのマスを横から見たイメージです。
このマス(大区画)は
- 縦:1 mm
- 横:1 mm
- 深さ:0.1 mm
となっており、血球計算盤の1マスの体積は 0.1 mm³(=0.1 μL)になります。
ここで重要になるのが、単位の変換です。
- 1 mm³ = 0.001 mL
- 1 mL = 1000 μL
したがって、1 mm³ = 1 μLとなります。
つまり、 0.1 mm³ = 0.1 μLとなります。
顕微鏡で見ているのは「平面」ですが、
実際に数えているのは「一定の体積の中にある細胞数」です。
この「体積」が決まっているからこそ、
「数えた細胞数」=「0.1 μL中の細胞数」と考えることができ、
そこから1 mLあたりの細胞数(cells/mL)に変換できるようになります。
なぜ「×10⁴」で細胞濃度が求まるのか
実際のカウントでは、この「1マス」を複数(例:4マス)数えます。
つまり、「0.1 μL × 4 = 0.4 μL中の細胞数」を見ていることになります。
本記事では、4つの大区画の合計値をそのまま用いて計算しています。
1 mLは 1000 μL なので、1000 μL ÷ 0.4 μL = 2500倍となります。
今回はチュルク液によって4倍に希釈しているため、
2500 × 4 = 10000 = 10⁴となります。
これにより細胞濃度(cells/mL)= カウント数 × 10⁴という計算式につながります。
つまり「小さい体積(0.4 μL)で見たものを、1 mLまで引き伸ばしている」というイメージです。
カウント値から細胞濃度を求める方法
細胞の数をカウントしたら、**目的の細胞数になるようにPBSで調整(希釈・濃縮)**します。
今回は、PBMC層をPBSで最終的に10 mLに調整し、血球計算盤で4マス数えた細胞数の合計が110個で、ここから2×10⁶個の細胞を取り出すという前提で説明します。
今回、4マス合計が110個だった場合、
110 × 10⁴ = 1.1 × 10⁶ cells/mLとなります。
これは、「1 mLの中に約110万個の細胞が含まれている」ということを意味します。
目的の細胞数(2×10⁶個)を取り出す計算方法
最終的にフローサイトメトリーで使用したい細胞数を、2×10⁶個とします。
この場合、必要な細胞溶液量は
使いたい細胞数 ÷ 現在の細胞濃度
で求めることができます。
今回の細胞濃度は 1.1 × 10⁶ cells/mLなので、
2×10⁶ ÷ 1.1 × 10⁶ = 約1.82 mL
となります。
つまり、 約1.82 mL分取すれば、その中に約200万個の細胞が含まれているということになります。
一般化すると
血球計算盤で4マスの合計を N個 とした場合、
① 細胞濃度
細胞濃度 = N × 10⁴ cells/mL
② 必要な細胞溶液量
必要量(mL) = 2×10⁶ ÷ (N × 10⁴)
これを整理すると、
必要量(mL) = 200 ÷ N
(※2×10⁶個を使用する場合)
例えば、4マス合計が 80個 の場合
200 ÷ 80 = 2.5 mL
- 4マス合計が 110個 の場合
200 ÷ 110 ≒ 1.82 mL
総細胞数を求める場合
もし、全体でどれくらいの細胞が取れているかを知りたい場合は、
総細胞数 = 細胞濃度 × 全量
で求めることができます。
今回のように、PBMC層を最終的にPBSで10 mLにしている場合、
- 4マス合計が110個
細胞濃度 = 1.1 × 10⁶ cells/mL
なので、総細胞数 = 1.1 × 10⁶ × 10 = 1.1 × 10⁷個
まとめると下記のようになります。
- カウント数 → 濃度(×10⁴)
- 濃度 → 必要量(200 ÷ N)
- 濃度 → 総細胞数(×全量)
すべて「細胞数」と「体積」の変換で説明できる
濃縮してから分取する方法(別解)
もう一つの考え方として、細胞を一度濃縮してから分取する方法があります。
PBMC分離後、PBSで調整して遠心する工程がありますが、
遠心の待ち時間に細胞数をカウントし、
遠心後に上清を除去して濃縮した細胞を、そのまま分取する方法です。
前提条件
- カウント結果:4マス合計 110個
- 最終的に 50 μL に再懸濁したとする
総細胞数を求める
まず、カウント結果から細胞濃度は
1.1 × 10⁶ cells/mLです。
全体をPBSで 10 mL にしている場合、
総細胞数 = 1.1 × 10⁶ × 10 = 1.1 × 10⁷個
濃縮後の細胞濃度(μLあたり)
この1100万個の細胞が、最終的に50 μLに入っているので、
濃縮後の濃度 = 1.1 × 10⁷ ÷ 50 μL
= 2.2 × 10⁵ cells/μL
これは1 μLあたり約22万個の細胞が含まれているということになります。
欲しい細胞数が 2×10⁶個 の場合、
必要量(μL) = 欲しい細胞数 ÷ 濃縮後の細胞数
なので、
2×10⁶ ÷ 2.2 × 10⁵ = 約9.1 μL
約9 μL分取すれば、約200万個の細胞が得られる
まとめると下記のようになります。
- 最初に「総細胞数」を出す
- それを「最終体積」で割る
- μLあたりの細胞数に変換する
あとは割り算するだけです。
結論:やっていることは1つだけ
細胞数の計算はシンプルで、「細胞数」と「体積」を変換しているだけです。
分取法と濃縮法の違い
実は、細胞の取り方には大きく2つの方法があります。
■ 分取派(わかりやすい)
- カウントする
- 必要量(例:1.8 mL)を取る
- それを遠心して使用する
直感的で理解しやすく、初心者向きの方法です。
■ 濃縮派(現場向き)
- 全量を遠心して濃縮する
- μL単位で必要量を分取する
作業効率が高く、再現性も取りやすい方法です。
細胞数計算の本質
この2つの方法は、一見違うように見えますが、やっていることは同じです。
どちらも最終的には、「2×10⁶個の細胞になるように調整する」のがゴールです。
両者の違いはここだけです。
- 分取派:👉 体積で合わせる
- 濃縮派:👉 濃度を上げてから体積で合わせる
ミニコラム①:なぜ「2×10⁶個」なのか?
フローサイトメトリーでは、「細胞は何個使えばいいのか?」と疑問に思う方も多いと思います。
結論から言うと、 2×10⁶個という数は絶対的な決まりではありません。
ではなぜ、このくらいの数が使われるのでしょうか。
理由①:十分なイベント数を確保するため
フローサイトメトリーでは最終的に、数千〜数万個の細胞を解析します。
しかしその過程で、
- 洗浄や遠心によるロス
- 死細胞の除外
- ゲーティングによる絞り込み
が起こります。
そのため、最初の細胞数が少ないと、最終的に解析に使える細胞数が不足する可能性があります。
理由②:希少細胞を評価するため
解析対象によっては、割合の低い細胞(希少細胞)を評価することがあります。
例えば、ある細胞が全体の1%しか存在しない場合、
- 10万個中 → 1000個
- 100万個中 → 1万個
と、母集団の大きさによって得られる情報量が大きく変わります。
理由③:抗体染色のバランス
抗体染色では、
- 細胞数
- 抗体量
- 反応体積
のバランスが重要です。
細胞数が多すぎると非特異的結合が増え、少なすぎると統計的な信頼性が低下します。
まとめ
このような理由から、フローサイトメトリーでは一般的に、
10⁵〜10⁶個程度の細胞がよく用いられます。
本記事では、その一例として2×10⁶個を用いて説明しています。
そのため、細胞数は「決まり」ではなく、「目的に応じた設定」です。
ミニコラム②:細胞数は切り捨てる
今回はカウントした細胞数が110個の場合で説明しましたが、
もし115個だった場合はどうするでしょうか?
この場合、116個に繰り上げるのではなく、
110個として切り捨てて考えるのがおすすめです。
その理由は、細胞数は少なめに見積もる方が安全だからです。
フローサイトメトリーでは、多すぎても少なすぎても適切な解析ができません。
特に、細胞数を多く見積もってしまうと、
- 必要以上に希釈してしまう
- 実際の細胞数が足りなくなる
といった問題が起こる可能性があります。
そのため、多少少なめに見積もる方が、実務上は扱いやすくなります。
※実際には厳密にぴったり合わせる必要はありませんが、安全側に寄せる意識が大切です。
まとめ
- 110個 → 1.1×10⁶ cells/mL
- 全量10 mL → 1.1×10⁷個
- 55 μLに濃縮 → 1 μLあたり約2×10⁵個
- 10 μL → 約2×10⁶個
つまり、約10 μL取ればOK
今日のおさらい
~ちょっと考えてみよう~
Q1
PBMCをPBSで最終的に10 mLにメスアップした後、血球計算盤で4マス合計が80個でした。
2×10⁶個の細胞を得るために必要な細胞溶液量は何mLですか?
※総細胞数は、メスアップした全量から求めるものとします。
Q2
同じ条件で(PBMCを10 mLに調整、4マス合計80個)、遠心後に上清を除去し、55 μLに再懸濁しました。
このとき、2×10⁶個の細胞を得るために必要な分取量は何μLですか?
答え:
A1:2.5 mL
4マス合計 = 80個
必要量(mL) = 200 ÷ N
= 200 ÷ 80 = 2.5 mL
A2:約14 μL
条件
- カウント:80個 → 濃度 = 80 × 10⁴ = 8.0 × 10⁵ cells/mL
- 全量:10 mL → 総細胞数 = 8.0 × 10⁶個
- 濃縮後:55 μL
① 濃縮後の濃度
8.0 × 10⁶ ÷ 55 μL
= 約 1.45 × 10⁵ cells/μL
② 必要量
2×10⁶ ÷ 1.45 × 10⁵
= 約 13.8 μL
計算は最初こそ難しく感じますが、自分の実験条件に合わせて一度計算式を作っておくと、次からはぐっと楽になります。


