スーパーやドラッグストアには、たくさんの洗剤が並んでいます。
クエン酸、重曹、セスキ、ハイター、酸素系漂白剤、パイプユニッシュ……。
名前は知っていても、「結局どれを、どんな汚れに使えばいいの?」と迷ったことはないでしょうか。
たとえば、水道まわりにつく白い汚れ。
私はこの記事を書くまで、恥ずかしながら「あれは塩素が固まったものだ」と思っていました。
でも実際には、あの白い汚れの正体は塩素ではありません。
炭酸カルシウム、つまり貝殻やサンゴと同じ成分です。
この記事では、汚れの種類と洗剤の性質を整理しながら、
何を解決したくてその洗剤を選ぶのか を、科学の視点でやさしく考えていきます。
洗剤は汚れの性質で選ぶ
洗剤を選ぶときに一番大切なのは、汚れの正体を知ることです。
汚れにはいくつかの種類があります。

そして、洗剤にもそれぞれ得意分野があります。
それぞれの汚れに対する洗剤はコレ!
結論から行きましょう。
それぞれの汚れに対する得意分野は下記の図の通りです。
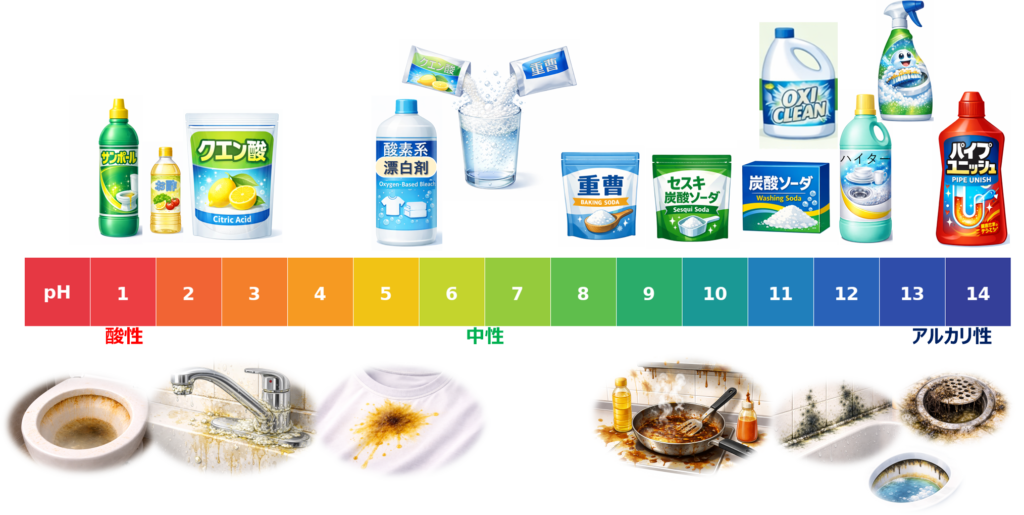
一覧にすると下記のようになります。
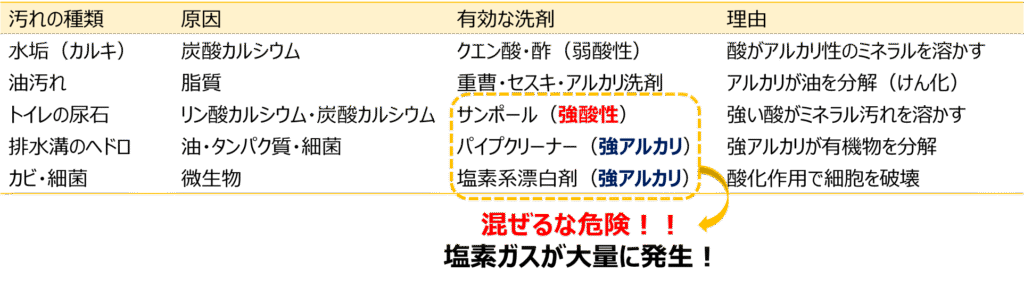
つまり、汚れの種類と洗剤のpHや成分によって使い分ける、ということです。
しかし、この表で終わってしまってはちょっとつまらないな、と思うので、今日はその理由を一つ一つ解説していきます。
トイレ用洗剤は「強い酸」または「塩素系のアルカリ洗剤」
トイレ用洗剤には、塩酸を主成分とするものがあります。
代表的な商品が サンポール です。
尿石などのカルシウム汚れを溶かすため、強い酸性になっています。
ただし、このような酸性洗剤をハイターなどの 塩素系漂白剤 と混ぜると、
塩素ガスが発生するため絶対に混ぜてはいけません。
ちなみに、便器の黒ずみに効く スクラビングバブル は、次亜塩素酸ナトリウムや水酸化ナトリウムを含む アルカリ性洗剤 です。
便器の黒ずみは
- 尿石(カルシウム汚れ)
- バイオフィルム(細菌の膜)
など、さまざまな汚れが混ざってできています。
そのため、トイレだから必ず酸性洗剤を使う というわけではありません。
各メーカーが表示している用途や成分を確認し、汚れに合わせて洗剤を使い分けることが大切です。
水垢(カルキ汚れ)には「弱酸」
ポットや蛇口につく白い汚れ。
これは「カルキ」と呼ばれることが多いですが、正体は炭酸カルシウム(CaCO₃)です。
水道水に含まれるミネラルが固まったもので、性質としてはアルカリ性の汚れになります。
ではなぜ、カルキを「塩素」と思っている人が多いのでしょうか。
それは、水道水のにおいをカルキ臭と呼ぶことに由来しています。
つまり「カルキ」という言葉は、実は2つの意味で使われています。
| 言葉 | 正体 |
|---|---|
| カルキ臭 | 塩素 |
| カルキ汚れ | 炭酸カルシウム |
においの原因は塩素ですが、蛇口やポットにつく白い汚れの正体は 炭酸カルシウム です。
なぜ炭酸カルシウムができるのか
水道水には
- カルシウム
- マグネシウム
などのミネラルが含まれています。
水が蒸発すると、これらのミネラルが残り炭酸カルシウムとして固まるのです。
簡単に書くと
Ca²⁺ + CO₃²⁻ → CaCO₃
これが
- ポットの白い汚れ
- 蛇口の白いウロコ
の正体です。
実は、ポットの中で起きている現象は、鍾乳洞とほぼ同じです。
鍾乳洞では、炭酸カルシウムが長い年月をかけて積み重なり「鍾乳石」になります。
ポットの白い汚れも、言ってみればそのミニチュア版。
つまりカルキ汚れは、台所にできた「小さな鍾乳石」とも言えるのです。
炭酸カルシウムはなぜアルカリ性?
ここで理系の方は、こんな疑問を持つかもしれません。
炭酸カルシウムは「塩」だから中性では?
実は炭酸カルシウムは中性ではなく弱いアルカリ性です。
なぜなら炭酸カルシウムは
| 物質 | 性質 |
|---|---|
| 水酸化カルシウム | 強塩基 |
| 炭酸 | 弱酸 |
からできているからです。
つまり弱酸 + 強塩基からできた塩になります。
塩が中性になる条件
塩が完全に中性になるのは強酸 + 強塩基からできた場合です。
例えば、塩酸と水酸化ナトリウムを反応させると、できるものはNaCl(食塩)と水です。
HCl + NaOH → NaCl + H₂O
食塩は完全に中性です。
弱酸由来の塩はアルカリ性になる
弱酸からできた塩は、水の中で少し分解します。
炭酸カルシウムの場合
CO₃²⁻ + H₂O ⇄ HCO₃⁻ + OH⁻
このとき OH⁻(水酸化物イオン) ができるため溶液はアルカリ性になります。
だからクエン酸が効く
炭酸カルシウムはアルカリ性なので酸で溶けます。
例えば
CaCO₃ + 2H⁺ → Ca²⁺ + CO₂ + H₂O
つまり
- 二酸化炭素(泡)
- 水
になって溶けます。
ポットをクエン酸で掃除するとシュワシュワするのはこの反応です。
水垢には弱酸が効く
アルカリ性の汚れを落とすには弱酸が効果的です。
代表的なものは
- クエン酸
- お酢
- 酸性洗剤
弱酸はカルシウムを溶かすため、水垢をきれいに落とすことができます。
油汚れには「アルカリ」
キッチンの油汚れや、皮脂汚れ。
これらの正体は脂質(油)です。
油汚れにはアルカリ性洗剤がよく効きます。
例えば
- 重曹
- セスキ炭酸ソーダ
- 炭酸ソーダ
などです。
アルカリは、油を分解して石けんのような物質に変える働きがあります。
この反応をけん化反応といいます。つまり、油とアルカリを反応させると石鹸になります。
脂肪 + アルカリ → 石けん + グリセリン
簡単に言うと、アルカリは油を水に溶けやすい形に変えてくれるのです。
昔の石けんは
- 動物の脂
- 木灰(アルカリ)
で作っていました。
つまり昔の人は油をアルカリで洗っていたということになります。
そのため、水では落ちにくい油汚れでも、アルカリ性洗剤を使うと落としやすくなります。
排水溝のヘドロには「強アルカリ」
排水溝の汚れは、実はかなり複雑です。
排水溝の中には
- 油
- 食べ物のカス
- タンパク質
- 細菌
などが混ざっています。つまり、排水溝のヘドロは有機物の塊と言えます。
これを分解するために使われるのがパイプユニッシュなどのパイプクリーナーです。
主成分は水酸化ナトリウム(NaOH)という非常に強いアルカリです。
この強アルカリは
- タンパク質
- 油
などの有機物を分解する働きがあります。
その結果、排水溝にたまったヘドロが分解され、詰まりが解消されるのです。
重曹などのアルカリでも油は落ちますが、排水溝のヘドロはそれだけでは分解しきれません。そのため、パイプクリーナーではより強力なアルカリが使われています。
※ただし、別の記事でも書いていますが、あまりにもお手入れしていない排水溝にパイプユニッシュを入れるのはお勧めしません。汚れが中途半端に剥がれ落ちて、排水溝詰まりの原因になる可能性があります。
水酸化ナトリウムは、タンパク質を分解し、油をけん化させるため、排水溝にたまった有機物を化学的に分解することができます。
つまりパイプユニッシュは溶かしているというより化学的に分解しているというイメージです。
アルカリ性といっても強さはさまざまで、重曹のような弱アルカリ(pH8〜9)から、パイプクリーナーのような強アルカリ(pH13以上)まであります。排水溝のヘドロのような頑固な有機汚れには、より強いアルカリが必要になります。
カビや菌には「塩素」
お風呂の黒カビに使うハイターやカビキラー。
これらは塩素系漂白剤と呼ばれる洗剤です。主成分は次亜塩素酸ナトリウムという物質です。この物質は非常に強い酸化作用を持っています。酸化とは、簡単に言うと分子を壊す力です。
この作用によって
- カビ
- 細菌
- 色素
この酸化作用によって、カビや細菌の細胞やタンパク質が破壊されます。
その結果、カビや菌を殺すことができるのです。
そのため、塩素系漂白剤は強力な除菌や漂白ができるのです。
ちなみにハイターはアルカリ性で、pH11〜13くらいです。
理由は次亜塩素酸ナトリウム(NaClO)がアルカリ性だからです。
水に溶けると
NaClO + H₂O ⇄ HOCl + NaOH
となり水酸化ナトリウム(NaOH)ができるためアルカリ性になります。
また、塩素を含んだ物質なので注意が必要です。
「混ぜるな危険」はなぜ危険?
洗剤にはよく「混ぜるな危険」という表示があります。
特に多いのが塩素系漂白剤です。
例えば
- ハイター
- カビキラー
などです。
では、なぜ混ぜてはいけないのでしょうか。
理由はとてもシンプルで、有毒なガスが発生するからです。
塩素ガスが発生する
塩素系漂白剤の主成分は次亜塩素酸ナトリウム(NaClO)です。
この物質はアルカリ性ですが、そこに酸性洗剤(塩酸など)が加わると化学反応が起こります。その結果、塩素ガス(Cl₂)が発生します。
反応を簡単に書くと
NaClO + 2HCl → Cl₂ + NaCl + H₂O
このとき発生する塩素ガスは強い刺激臭を持つ有毒ガスです。
吸い込むと
- 咳
- 目の痛み
- 呼吸困難
などを引き起こします。
そのため塩素系洗剤と酸性洗剤は絶対に混ぜてはいけません。
なぜお風呂で事故が起きやすいのか
実はこの事故、お風呂掃除で起きることが多いです。
例えば
- カビキラー(塩素系)を使う
- 水垢を落とすためクエン酸を使う
この2つが混ざると塩素ガスが発生します。
クエン酸は弱い酸で、塩素そのものを含んでいるわけではありません。
一方、ハイターなどの塩素系漂白剤の主成分である次亜塩素酸ナトリウムには塩素が含まれています。
次亜塩素酸ナトリウムはアルカリ性では安定していますが、そこに酸を加えると反応が起こり塩素ガス(Cl₂)が発生します。
そのため、クエン酸のような弱酸でも塩素系漂白剤と混ざると塩素ガスが発生する可能性があります。
特に、サンポールのような塩酸を主成分とする強酸性洗剤と混ざると大量の塩素ガスが発生し非常に危険です。
そのため塩素系漂白剤と酸性洗剤は絶対に混ぜてはいけません。
しかも浴室は密閉空間なので危険度が上がります。
そのため洗剤には「混ぜるな危険」と大きく表示されているのです。
実は、第一次世界大戦で化学兵器として使われたのも
この塩素ガスです。
酸素系漂白剤とは?
もう一つよく見かけるのが酸素系漂白剤です。
代表例は
- オキシクリーン
- 過炭酸ナトリウム
これらは水に溶けると炭酸ナトリウムと過酸化水素に分かれます。
この炭酸ナトリウムのアルカリと過酸化水素が色素を分解して、汚れを落とします。
塩素系と違い
- 色柄ものに使える
- においが弱い
という特徴があり、衣服の漂白に使います。
クエン酸と重曹を混ぜるとどうなる?
SNSなどでよく紹介されるクエン酸+重曹ですが、実はこの組み合わせには少し誤解があります。
この2つを混ぜると、シュワシュワと泡が発生します。
これは 二酸化炭素(CO₂) が発生しているためです。
反応を簡単に書くと
重曹 + クエン酸
↓
二酸化炭素 + 水 + クエン酸ナトリウム
という化学反応が起きています。
つまり、この泡の正体は二酸化炭素のガスです。
反応が終わったあとに残るのはクエン酸ナトリウムというほぼ中性の物質になります。
そのため、この組み合わせは強い洗浄力があるわけではありません。
主な効果は発泡によって汚れを浮かせることです。
もちろん、泡の力で軽い汚れを浮かせる効果はありますが、クエン酸や重曹をそれぞれ単独で使ったときほどの化学的な洗浄力は期待できません。
まとめ
ここまで整理すると、洗剤は「場所」ではなく 汚れの性質で選ぶと、効率よく掃除することができます。
酸はミネラル汚れ、アルカリは油汚れ、塩素は微生物に効く――この基本を覚えておくと、洗剤選びがとてもシンプルになります。

汚れの正体と洗剤の成分がわかれば、どんな洗剤を使えばいいかは自然と見えてきます。
生活の中にも、ちょっとした化学が隠れているんですね。
今日のおさらい
~ちょっと考えてみよう~
Q1.ポットや蛇口につく白い水垢(カルキ)の主成分は何でしょう?
A. 塩素
B. 炭酸カルシウム
C. 塩化ナトリウム
Q2.キッチンの油汚れを落とすのに向いている洗剤はどれでしょう?
A. クエン酸
B. 重曹
C. お酢
Q3.次のうち、絶対に混ぜてはいけない組み合わせはどれでしょう?
A. クエン酸 + 重曹
B. ハイター + 酸性洗剤
C. 重曹 + セスキ炭酸ソーダ
答え
Q1 → B(炭酸カルシウム)
水垢は水道水中のミネラルが固まったものです。
Q2 → B(重曹)
油汚れにはアルカリ性洗剤が効果的です。
Q3 → B(ハイター+酸性洗剤)
塩素ガスが発生する危険があります。

